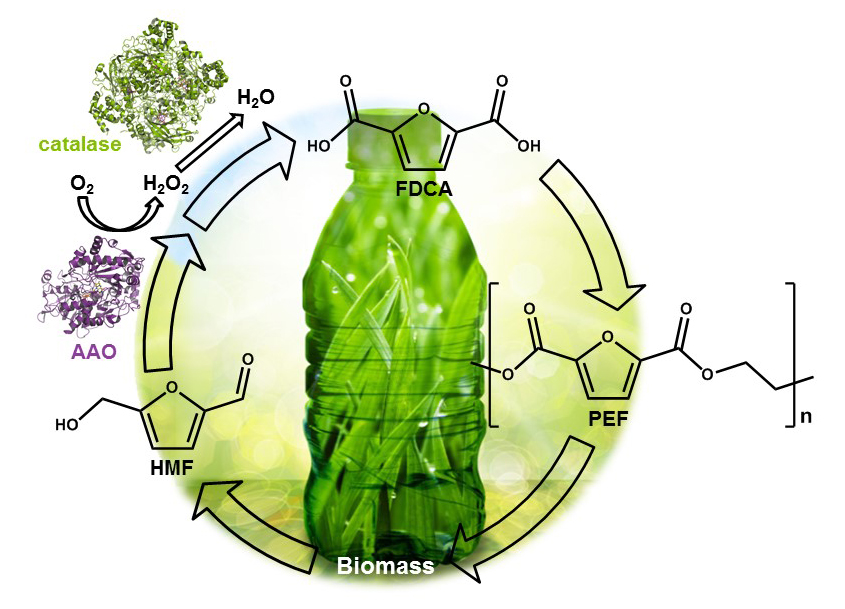
Investigadores del grupo de Biotecnología para la Biomasa Lignocelulósica del Centro de Investigaciones Biológicas, en colaboración con el grupo de RMN y Reconocimiento Molecular de este mismo centro, han logrado recientemente la oxidación completa de 5-hidroximetilfurfural (HMF) a ácido 2,5-furandicarboxílico (FDCA) catalizado por la enzima aril-alcohol oxidasa (AAO), un tipo de oxidasa que actúa sobre los grupos alcohol y aldehído de los compuestos bencílicos. Este trabajo se ha llevado a cabo en el marco del proyecto europeo EnzOx2, que se centra en el desarrollo de nuevas tecnologías bioquímicas para la producción de compuestos de alto valor añadido a partir de componentes de la biomasa.
El HMF, que puede obtenerse a partir de carbohidratos de biomasa vegetal mediante tratamientos de hidrólisis, isomerización y deshidratación, constituye una plataforma química altamente valiosa. El HMF se puede oxidar a FDCA, un compuesto clasificado como uno de los 12 productos químicos de mayor valor añadido derivados de la biomasa, por ser el precursor renovable del poli(2,5-furandicarboxilato de etileno) (PEF), el polímero que se espera sustituya a los plásticos de poli(tereftalato de etileno) (PET) derivados del petróleo en un futuro cercano. Por esta razón, la búsqueda de métodos viables de producción de FDCA a partir de biomasa lignocelulósica suscita gran interés en los últimos años, incluyendo los métodos biotecnológicos como alternativa a la síntesis química.
La conversión de HMF en FDCA implica tres pasos de oxidación consecutivos, con varias enzimas capaces de catalizar algunas de las reacciones individuales. Por un lado, algunas oxidasas actúan sobre los grupos alcohol o aldehído de estos compuestos, requiriendo solo oxígeno molecular como cosustrato. Por otro lado, algunas peroxidasas/peroxigenasas pueden hidroxilar algunos de estos compuestos a expensas de peróxido de hidrógeno. En este contexto, se han utilizado combinaciones de varias de estas enzimas para la producción de FDCA a partir de HMF. Sin embargo, la aplicación de cascadas enzimáticas presenta algunas desventajas, como la necesidad de combinar las diferentes condiciones operativas óptimas de cada enzima (por ejemplo, pH y temperatura).
Se sabía que la enzima AAO utilizada en este trabajo cataliza eficientemente los dos primeros pasos en la conversión de HMF a FDCA, pero no puede realizar la última reacción de oxidación, conduciendo a la acumulación de ácido 2,5-formilfurancarboxílico (FFCA). En este estudio, los investigadores de CIB indagaron en las razones de esta falta de actividad y descubrieron que el peróxido de hidrógeno, subproducto de las dos primeras oxidaciones catalizadas por la enzima, inhibía la oxidación de FFCA, evitando la producción del producto deseado, FDCA. Las reacciones en tiempo real en ausencia y en presencia de catalasa monitorizadas mediante experimentos de H1-RMN confirmaron la producción de FDCA cuando el peróxido de hidrógeno era eliminado por la acción de la catalasa. El control de los niveles de peróxido de hidrógeno durante la reacción, al agregar catalasa, resultó en una conversión del 99% de HMF en FDCA por AAO. Además, bajo estas condiciones, diferentes variantes de enzimas diseñadas para mejorar el rendimiento consiguieron aumentar la velocidad del último paso de oxidación, disminuyendo consecuentemente los tiempos de reacción y proporcionando mayores conversiones.
Finalmente, los autores también analizaron en más detalle la oxidación de FFCA a FDCA por AAO, descubriendo que ésta no se produce siguiendo el mecanismo común en dos pasos que libera peróxido de hidrógeno, sino que se realiza a través de un nuevo mecanismo de oxigenación no descrito hasta ahora para esta enzima.
El proyecto EnzOx2 ha recibido financiación de Bio Based Industries Joint Undertaking en el marco del Programa de Investigación e Innovación Horizonte 2020 de la Unión Europea, en virtud del acuerdo de subvención nº 720297.
Referencia: Complete oxidation of hydroxymethylfurfural to furandicarboxylic acid by aryl-alcohol oxidase. Serrano A, Calviño E, Carro J, Sánchez-Ruiz MI, Cañada FJ, Martínez AT (2019) Biotechnol. Biofuels, 12: 127. https://doi.org/10.1186/s13068-019-1555-z

