Un trabajo publicado en J. Med. Chem. por el grupo de Agentes estabilizantes de microtúbulos dirigido por el Dr. Fernando Díaz en el Centro de Investigaciones Biológicas Margarita Salas (CIB-CSIC), ha proporcionado información estructural de la unión de noscapina a tubulina permitiendo proponer un mecanismo para su actividad como agente anticancerígeno.
La noscapina es un alcaloide natural que se usa como medicamento antitusivo. Sin embargo, también actúa como un agente anticancerígeno débil, no tóxico, en ciertos modelos a través de un mecanismo que es en gran medida desconocido. Este trabajo, que resulta de una colaboración internacional, muestra que el agente citotóxico 7A-O-dimetoxi-amino-noscapina (7A-amino-noscapina) se une al sitio de colchicina de la tubulina.
Oliva et al. proponen que la actividad anticancerígena de la noscapina surge de un metabolito bioactivo que se une al sitio de colchicina de la tubulina para inducir el paro mitótico a través de los microtúbulos en un mecanismo basado en el citoesqueleto.
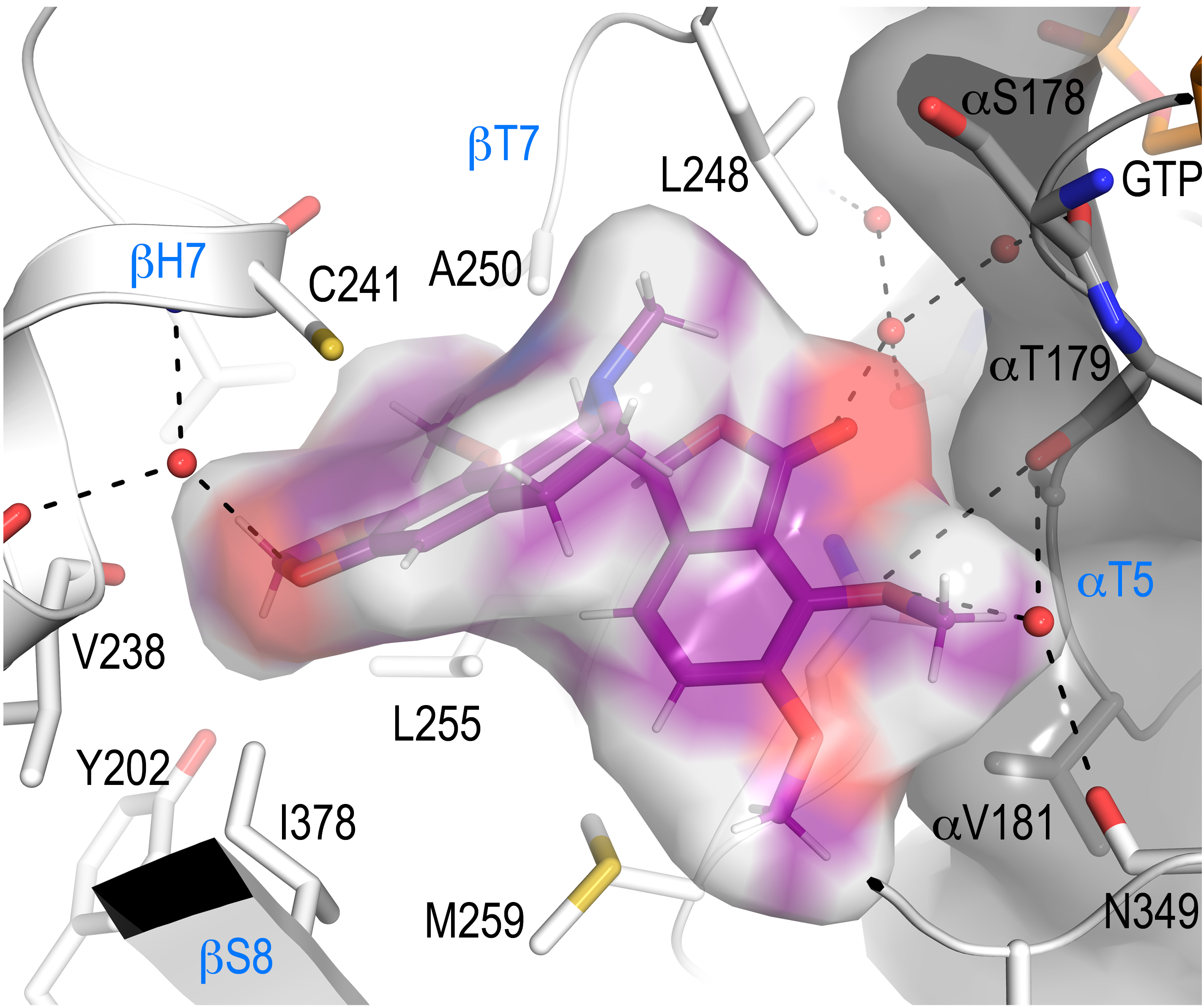
Se ha construido un modelo tridimensional basado en docking asistido por RMN, combinando datos de STD y cálculos de CORCEMA-ST, validado mediante la determinación de la estructura del complejo tubulina-7A-amino-noscapina por cristalografía de rayos x, que indica que el grupo 7A-metoxi de la noscapina evita la unión a la tubulina debido a un choque estérico del compuesto con el loop T5 de α-tubulina.
Los autores proponen que la citotoxicidad de la noscapina es una consecuencia de la oxidación de su carbono metoxi en posición 7A, lo que conduce a la formación de un fenol activo. El fármaco resultante puede unirse a la tubulina y bloquear el ensamblaje de los microtúbulos de manera similar a la colchicina.
En este sentido, y al contrario de lo que sucede con la colchicina, el otro compuesto dirigido a tubulina utilizado como inmunomodulador, la noscapina no es tóxica, lo que permite su uso en dosis altas, abriendo un amplio abanico de posibilidades terapéuticas para este medicamento.
Referencia: Structural basis of noscapine activation for tubulin binding. Maria A. Oliva, Andrea E. Prota, Javier Rodríguez-Salarichs, Youssef L. Bennani, Jesús Jiménez-Barbero, Katja Bargsten, Angeles Canales, Michel O. Steinmetz, and J. Fernando Díaz (2020) J. Med. Chem. https://doi.org/10.1021/acs.jmedchem.0c00855

